- 試験デザイン
- PEACE-3試験とERA223試験
- 患者背景
- 治療状況
- rPFS[主要評価項目、検証的解析結果]
- rPFSのサブグループ解析
- OS[重要な副次評価項目、最終解析]
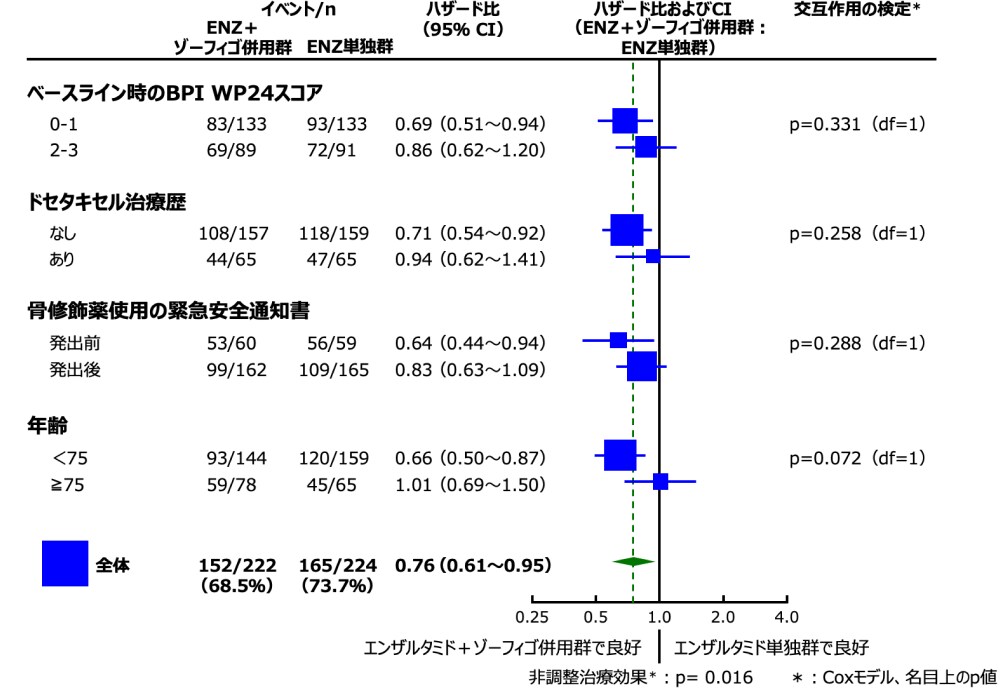
- OSのサブグループ解析
- 次治療開始までの期間[重要な副次評価項目]
- 次治療の内訳
- 重要な副次評価項目(一覧)
- 有害事象
- 骨折(有害事象)の発現状況
- 骨折事象の詳細#
- 骨折初回発現までの期間[安全性評価項目]
- まとめ
- ゾーフィゴ適正使用ガイド 補遺
- 患者登録基準
#Worst grade of treatment-emergent AE として記録された骨折事象の詳細
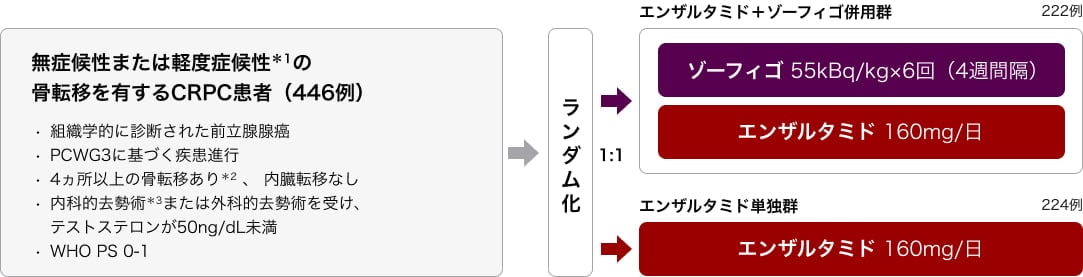
*1:簡易疼痛質問票で評価した直近24時間の最悪疼痛スコア(BPI WP24)<4
*2:2018年に、2ヵ所以上から4ヵ所以上に変更
*3:LHRHアゴニストまたはアンタゴニストによる継続的アンドロゲン遮断療法(ADT)
ERA223試験の高い骨折率の懸念に基づく盲検解除を受け、骨修飾薬(ビスホスホネート、デノスマブ)の併用を必須とするプロトコル改訂を実施(2018年4月、119例の患者登録後)
層別化因子:国、ベースライン時のBPI WP24(0-1 vs 2-3)、ドセタキセル治療歴(あり vs なし)、骨修飾薬使用の有無(使用なし or ≦4週間 vs >4週間)、アビラテロン治療歴(あり vs なし)
| 目的 | 無症候性または軽度症候性の骨転移を有するCRPC患者を対象に、エンザルタミド単独療法に対するエンザルタミド+ゾーフィゴ併用療法の有用性を検証する。 |
|---|---|
| 主要評価項目 | 画像判定に基づく無増悪生存期間(rPFS)*4[検証的解析項目] |
| 重要な副次評価項目 | 全生存期間(OS)、次治療開始までの期間(TTNT)、疼痛増悪までの期間(TTPP)、症候性骨関連事象(SSE)初回発現までの期間 |
| その他の副次評価項目 | 二次治療における無増悪生存期間、オピオイド使用までの期間 、前立腺癌特異的生存期間 、骨病変進行までの期間 、EQ-5D-5LによるQOLなど |
| 安全性評価項目 | 試験治療下で発現した有害事象、骨折の発現率、骨折初回発現までの期間など |
| 解析計画 |
|
*4:画像判定に基づく無増悪生存期間(rPFS)の定義:
治験医師評価による、ランダム化から、PCWG3に基づく最初の増悪またはあらゆる原因による死亡までの期間。
増悪の評価は、骨シンチグラフィー、胸部、腹部、骨盤部の造影CTまたはMRIを用いて実施し、増悪イベントは以下のいずれかとした。
- 軟部組織病変に関するRECISTv1.1に準拠した客観的疾患進行
- 2つ以上の新たな骨病変の出現を増悪とするが、左記の出現が初回の評価時点(治療開始12週間以内±1週間以内、すなわちフレアが起こり得る期間内)であった場合のみ、6週間以上経過後に実施されるスキャンにおいて2つ以上の追加の新病変が確認されることをもって増悪とする(2+2ルール)
- CRPC :去勢抵抗性前立腺癌
- PCWG3 :Prostate Cancer Working Group3
- LHRH :黄体形成ホルモン放出ホルモン
Tombal B, et al.: Ann Oncol. 36; 1058-1067, 2025.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。)
| PEACE-3試験1,2,5)*1 | ERA223 試験3)*2 | |
|---|---|---|
| 登録期間 | 2015/11 – 2023/03 | 2014/03 – 2016/08 |
| データカットオフ日 | 主解析 2024/2/19、最終解析 2025/5/1 | 2018/2/15 |
| デザイン | 第Ⅲ相、ランダム化、非盲検、実薬対照 | 第Ⅲ相、ランダム化、二重盲検、プラセボ対照 |
| 患者登録基準(抜粋) |
|
|
| 投与群 | 試験薬群:エンザルタミド+ゾーフィゴ 対照薬群:エンザルタミド | 試験薬群:ゾーフィゴ+アビラテロン+prednisone*4/ プレドニゾロン/ 対照薬群:プラセボ +アビラテロン+prednisone*4/ プレドニゾロン |
| 主要評価項目 | 画像判定に基づく無増悪生存期間 (rPFS) | 症候性骨関連事象無発症生存期間 (SSE-FS) |
| 骨修飾薬 | 治験医師の判断(~2018) 必須(2018~) | ベースライン時点で投与されている患者 のみ継続使用が許容 |
*1:国外試験(海外データ)
*2:国際共同試験(海外データ、日本人を含む)
*3:DEXA:二重エネルギーX線吸収測定法
*4:国内未承認
出典より作表
ゾーフィゴ静注 電子添文[2025年3月改訂(第2版、再審査結果)]
7. 用法及び用量に関連する注意(抜粋):7.3 化学療法未治療で無症候性又は軽度症候性の骨転移のある去勢抵抗性前立腺癌患者に対する本剤とアビラテロン酢酸エステル及びプレドニゾロンの併用投与は推奨されない。[15.1.2参照]
1)Tombal B, et al.: Ann Oncol. 36; 1058-1067, 2025.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。)
2)Gillessen S, et al.: Eur Urol. 87: 285-288, 2025(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料、コンサルタント料等を受領している者が含まれる。)
3)Smith M, et al.: Lancet Oncol. 20; 408-419, 2019.(本研究はバイエルの資金により実施された。著者には、バイエルから講演料・コンサルタント料等を受領した者、およびバイエルの社員5名が含まれる。)
4)WHO Techincal Report Series 843
5)Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、バイエルから講演料・コンサルタント料等を受領した者が含まれる。)
| エンザルタミド+ゾーフィゴ 併用群 (n=222) | エンザルタミド 単独群 (n=224) | 全体 (n=446) | |
|---|---|---|---|
| 年齢、中央値(範囲) | 70.0歳(43.0~90.0) | 70.0歳(47.0~90.0) | 70.0歳(43.0~90.0) |
| 初回診断からの期間、中央値(範囲) | 3.5年(0.1~22.4) | 2.9年(0.5~28.1) | 3.3年(0.1~28.1) |
| 転移性前立腺癌の診断からの期間、中央値(範囲) | 1.5年(0.0~18.1) | 1.5年(0.0~28.1) | 1.5年(0.0~28.1) |
| ADT開始からの期間 、中央値(範囲) | 1.9年(0.0~19.6) | 1.8年(0.0~14.4) | 1.8年(0.0~19.6) |
| ベースライン時の疼痛スコア、n(%) | |||
| BPI WPスコア 0-1 | 122(55.0) | 121(54.0) | 243(54.5) |
| BPIWPスコア 2-3 | 79(35.6) | 89(39.7) | 168(37.7) |
| BPI WPスコア >3 | 9(4.1) | 10(4.5) | 19(4.3) |
| 欠測 | 12(5.4) | 4(1.8) | 16(3.6) |
| ランダム化前のデノスマブまたはビスホスホネートの 使用(>4週間)、n(%) | 77(34.7) | 77(34.4) | 154(34.5) |
| ドセタキセル治療歴*、n(%) | 67(30.2) | 66(29.5) | 133(29.8) |
| アビラテロン治療歴*、n(%) | 4(1.8) | 7(3.1) | 11(2.5) |
| WHO PS 0、n(%) | 153(68.9) | 154(68.8) | 307(68.8) |
| Gleasonスコア、n(%) | |||
| <8 | 82(36.9) | 73(32.6) | 155(34.8) |
| ≧8 | 138(62.2) | 147(65.6) | 285(63.9) |
| 欠測 | 2(0.9) | 4(1.8) | 6(1.3) |
| ランダム化時のステージN1、n(%) | 56(25.2) | 51(22.8) | 107(24.0) |
| ランダム化時のステージM1b、n(%) | 221(99.5) | 223(99.6) | 444(99.6) |
| 限局性骨病変*1、n(%) | |||
| 0(限局性骨病変なし) | 19(8.6) | 19(8.5) | 38(8.5) |
| <10 | 109(49.1) | 105(46.9) | 214(48.0) |
| ≧10 | 93(41.9) | 99(44.2) | 192(43.0) |
| 欠測 | 1(0.5) | 1(0.4) | 2(0.4) |
| ランダム化時のステージM1c、n(%)*2 | 1(0.5) | 1(0.4) | 2(0.4) |
| ベースライン時の骨外性病変、n(%) | 77(34.7) | 73(32.6) | 150(33.6) |
| PSA、中央値(Q1~Q3)、ng/mL | n=190 24.5(7.8~68.8) | n=191 21.2(7.9~53.1) | n=381 22.4(7.9~62.0) |
| ALP*3、中央値(Q1~Q3)、IU/L | n=207 106.0(78.0~183.0) | n=218 124.5(85.0~216.0) | n=425 119.0(81.0~203.0) |
*:前治療としてのドセタキセルまたはアビラテロンは、ADT併用での転移性去勢感受性前立腺癌(mCSPC)に対する治療の場合に許容された。
*1:EORTC画像診断ガイドラインに従い、放射線科医が骨病変の種類を報告し、限局性、びまん性または不明瞭のいずれかに分類する。骨シンチグラフィーで特定可能な限局性骨病変のみがカウントされる。
*2:ゾーフィゴは内臓転移のある前立腺癌における有効性及び安全性は確立していない。
*3:IFCC法
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、バイエルから講演料・コンサルタント料等を受領した者が含まれる。)
- ゾーフィゴの6回投与完遂率は88.4%であった。
- エンザルタミド+ゾーフィゴ併用群のエンザルタミド治療期間の中央値は20.1ヵ月、エンザルタミド単独群は14.7ヵ月であった。
- 最終解析時点で、エンザルタミド投与はエンザルタミド+ゾーフィゴ併用群29例(13.3%)、エンザルタミド単独群28例(12.5%)で継続していた。
データカットオフ日:2025年5月1日
| エンザルタミド+ゾーフィゴ 併用群* | エンザルタミド 単独群 | |
|---|---|---|
| ゾーフィゴ投与回数 | n=215 | |
| 6回、n(%) | 190(88.4) | ー |
| 5回、n(%) | 4(1.9) | ー |
| <5回、n(%) | 21(9.8) | ー |
| エンザルタミド治療期間 | n=218 | n=224 |
| 中央値(範囲) | 20.1ヵ月(1.1~87.8) | 14.7ヵ月(0.2~85.7) |
- * :エンザルタミド+ゾーフィゴ併用群へ割り付けられた222例中、4例(1.8%)がいずれの試験治療も実施されず、3例(1.3%)はエンザルタミドのみ投与された。
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、バイエルから講演料・コンサルタント料等を受領した者が含まれる)より作表
- ・ エンザルタミド単独群に対するエンザルタミド+ゾーフィゴ併用群の優越性が検証された(ハザード比0.69、p=0.0009)。
- ・ rPFS中央値はエンザルタミド+ゾーフィゴ併用群で19.4ヵ月、エンザルタミド単独群で16.4ヵ月であった。
![rPFS[主要評価項目、検証的解析結果]](/sites/g/files/vrxlpx13761/files/2025-07/doctor__product__performance__peace3__image-02.png)
https://creativecommons.org/licenses/by/4.0/
追跡期間中央値:エンザルタミド+ゾーフィゴ併用群42.3ヵ月、エンザルタミド単独群41.1ヵ月、データカットオフ日:2024年2月19日
Tombal B, et al.: Ann Oncol. 36; 1058-1067, 2025.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。)
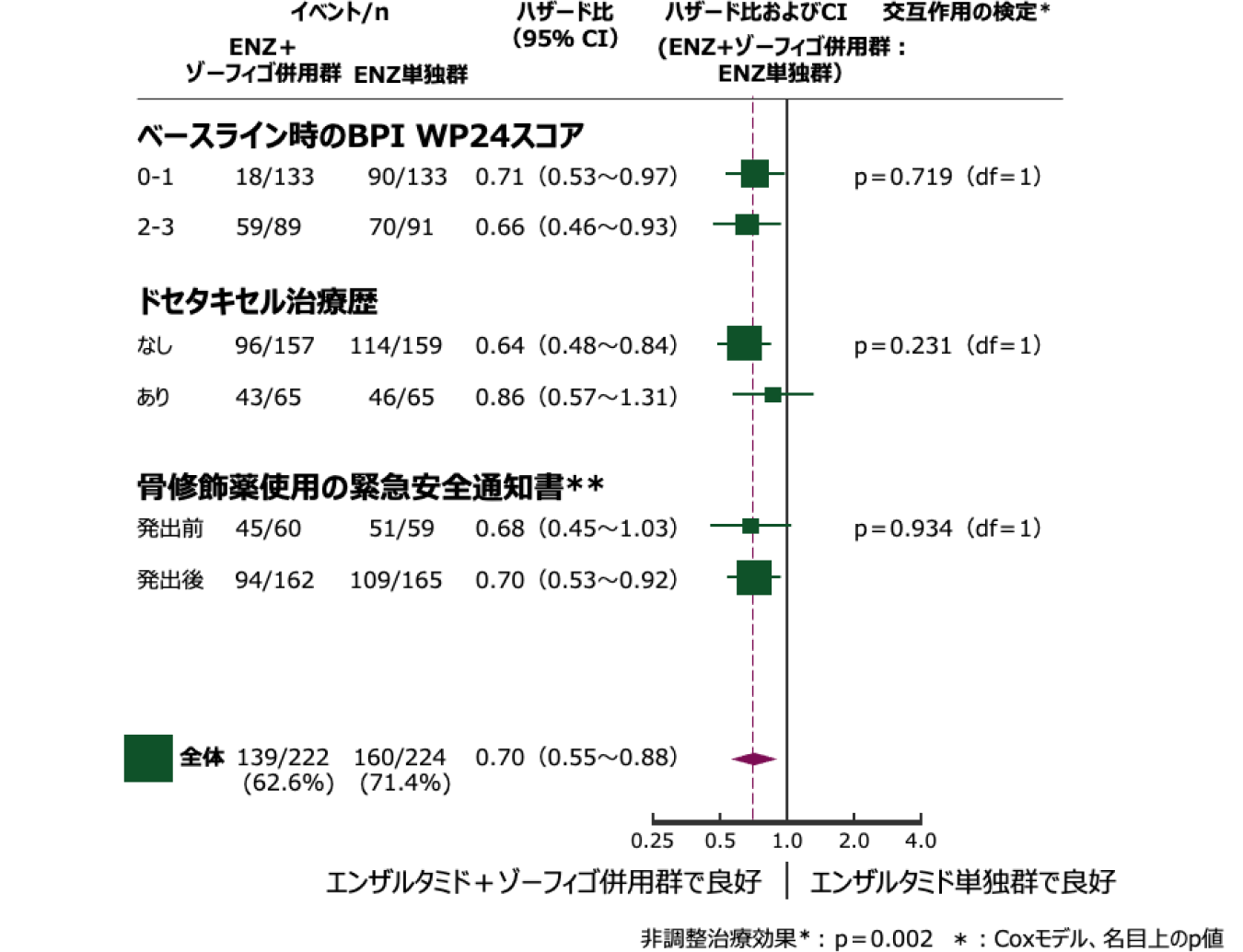
- rPFSに対する治療効果(ハザード比)は、解析対象となった全てのサブグループで一貫していた。
https://creativecommons.org/licenses/by/4.0/
- ENZ: エンザルタミド
- df: 交互作用の自由度
- **: 事後解析であるが、安全性確保を目的とした当該情報が試験結果に及ぼした影響を検討することの重要性を考慮し情報提供する。
Tombal B, et al.: Ann Oncol. 36; 1058-1067, 2025.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。)
- エンザルタミド+ゾーフィゴ併用群は、エンザルタミド単独群よりもOSが延⻑した(ハザード比 0.76、p=0.0096*)。
- OS中央値は、エンザルタミド+ゾーフィゴ併用群で38.2ヵ月、エンザルタミド単独群で32.6ヵ月であった。
![OS[重要な副次評価項目、最終解析]](/sites/g/files/vrxlpx13761/files/2026-03/doctor_product_performance_peace3-img-new-01.png)
追跡期間中央値:58.0ヵ月、データカットオフ日:2025年5月1日
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、バイエルから講演料・コンサルタント料等を受領した者が含まれる。)
- エンザルタミド+ゾーフィゴ併用群とエンザルタミド単独群の生存期間(曲線下面積)の差は、54.7ヵ月時点*1で73.1日、68.0ヵ月時点*2で115.1日、93.4ヵ月時点で195.9日であった。
| 期間 | 設定根拠 | 層別*3解析 | 曲線下面積の差 (エンザルタミド+ゾーフィゴ併用群 ーエンザルタミド単独群) | 両側p値*4 |
|---|---|---|---|---|
| 1571日(51.6ヵ月) | Max allowed by strata | あり | 27.3日 | 0.593 |
| 1571日(51.6ヵ月) | Max allowed by strata | なし | 60.8日 | 0.179 |
| 1664日(54.7ヵ月)*1 | 15%リスクセット | なし | 73.1日 | 0.131 |
| 2070日(68.0ヵ月)*2 | 7.5%リスクセット | なし | 115.1日 | 0.061 |
| 2843日(93.4ヵ月) | Max total | なし | 195.9日 | 0.015 |
*1:残った患者が15%となった時点からの近似月
*2:残った患者が7.5%となった時点からの近似月
*3:層別化因子:ベースライン時の疼痛スコア、ドセタキセル治療歴、ランダム化時に報告された骨修飾薬の使用状況
*4:χ2 test、有意水準:両側0.05、名目上のp値
※:RMST(Restricted Mean Survival Time)は「境界時間内でのイベント発現までの時間に対する平均値」と定義され、比例ハザード性が成立しないと想定される場合の生存時間型応答の評価指標の一つ1)。
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、
バイエルから講演料・コンサルタント料等を受領した者が含まれる。)
1)長谷川貴大. 癌と化学療法. 49; 389-396, 2022.
- エンザルタミド単独群に対するエンザルタミド+ゾーフィゴ併用群のハザード比は0.61(95% CI:0.48~0.78)であった。
- 36ヵ月時点の次治療開始率は、エンザルタミド+ゾーフィゴ併用群で44.5%、エンザルタミド単独群で65.2%であった。
![次治療開始までの期間[重要な副次評価項目、探索的解析結果]](/sites/g/files/vrxlpx13761/files/2026-03/doctor_product_performance_peace3-img-new-03.png)
追跡期間中央値:58.0ヵ月、データカットオフ日:2025年5月1日
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、 バイエルから講演料・コンサルタント料等を受領した者が含まれる。)
病勢進行例に対する次治療は以下のとおりであった。
| 次治療 | エンザルタミド+ゾーフィゴ 併用群 | エンザルタミド 単独群 |
|---|---|---|
| 化学療法(他治療の併用の有無は問わない) | 73例(75.3%) | 99例(70.7%) |
| ホルモン療法 | 15例(15.5%) | 18例(12.9%) |
| PARP阻害薬 | 2例(2.1%) | 3例(2.1%) |
| その他 | 2例(2.1%) | 13例(9.3%) |
PARP:poly ADP-ribose polymerase
Tombal B, et al.: Ann Oncol. 36; 1058-1067, 2025.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。)
重要な副次評価項目の結果は以下のとおりであった。
| 重要な副次評価項目 | エンザルタミド+ ゾーフィゴ併用群 (n=222) | エンザルタミド 単独群 (n=224) | ハザード比 [95% CI] | p値 | |
|---|---|---|---|---|---|
| OS | 中央値[95% CI] | 38.2ヵ月 [33.1~44.8] | 32.6ヵ月 [29.3~38.2] | - | - |
| イベント数/症例数 | 152/222 | 165/224 | 0.76 [0.60~0.96] | 0.0096a | |
| 次治療開始までの期間 | 次治療開始率(36ヵ月時点) [95% CI] | 44.5% [37.7~51.0] | 65.2% [58.3~71.3] | - | - |
| イベント数/症例数 | 116/222 | 151/224 | 0.61 [0.48~0.78] | -c | |
| 疼痛増悪までの期間 | 疼痛増悪率(36ヵ月時点) [95% CI] | 52.5% [44.8~59.7] | 50.9% [43.2~58.2] | - | - |
| イベント数/症例数 | 95/192b | 96/194b | 1.01 [0.76~1.33] | -c | |
| SSE初回発現までの期間 | SSE初回発現率(36ヵ月時点) [95% CI] | 21.5% [16.3~27.2] | 21.0% [15.9~26.7] | - | - |
| イベント数/症例数 | 52/222 | 48/224 | 1.08 [0.74~1.59] | -c |
データカットオフ日:2025年5月1日
a:層別※log-rank test(片側検定)
b:疼痛評価対象集団:ベースライン時にオピオイドが投与されておらず、ベースライン時のBPI WP24スコアが9未満であった患者
c:OS以外の重要な副次評価項目は、主解析時にゲートキーピング法を用いた階層的手順に従い検定を実施したが、OS最終解析時には探索的解析のため検定を実施しなかった。
※:層別化因子:ベースライン時の疼痛スコア、ドセタキセル治療歴、ランダム化時に報告された骨修飾薬の使用状況
追跡期間中央値:58.0ヵ月
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、バイエルから講演料・コンサルタント料等を受領した者が含まれる。)より作表
| 有害事象 CTCAE ver. 4.03 | エンザルタミド+ゾーフィゴ併用群 (n=218) | エンザルタミド単独群 (n=224) | ||
|---|---|---|---|---|
| 全グレード | グレード≧3 | 全グレード | グレード≧3 | |
| 全有害事象、n(%) | 218(100) | 151(69.3) | 219(97.8) | 129(57.6) |
| 重篤な有害事象、n(%) | 107(49.1) | 73(33.5) | 73(32.6) | 43(19.2) |
| 死亡に至った有害事象、n(%) | 8(3.7) | 8(3.7) | 6(2.7) | 6(2.7) |
| 中止に至った有害事象、n(%) | 12(6.3) | ー | 12(6.1) | ー |
- *1: ランダム化された患者のうち、少なくとも1種類の試験治療薬を1回以上投与された患者
- *2: 試験治療下で発現した有害事象[試験治療中(投与開始日から最終投与後28日まで)に発現または悪化した有害事象]
死亡に至った有害事象 (重複あり)
[エンザルタミド+ゾーフィゴ併用群:急性心筋梗塞 1例(0.5%)、心停止 2例(0.9%)、心原性ショック 1例(0.5%)、心筋梗塞 1例(0.5%)、Covid-19 1例(0.5%)、敗血症性ショック 1例(0.5%)、脳出血 1例(0.5%)、自殺 1例(0.5%)、肺臓炎 1例(0.5%)]
[エンザルタミド単独群:腸閉塞 1例(0.4%)、多臓器不全症候群 1例(0.4%)、敗血症 1例(0.4%)、脳出血 1例(0.4%)、脳血管障害 1例(0.4%)、意識レベルの低下 1例(0.4%)]
本論文には、重篤な有害事象名、投与中止に至った有害事象名の記載はないため、各薬剤の安全性に関する情報は、最新の電子添文をご参照ください。
| 有害事象 CTCAE ver. 4.03 | エンザルタミド+ゾーフィゴ併用群 (n=218) | エンザルタミド単独群 (n=224) | ||
|---|---|---|---|---|
| 全グレード | グレード≧3 | 全グレード | グレード≧3 | |
| いずれかの群で>10%発現した有害事象、n(%) | ||||
| 高血圧 | 122(56) | 78(35.8) | 136(60.7) | 80(35.7) |
| 疲労 | 86(39.4) | 12(5.5) | 87(38.8) | 4(1.8) |
| 体重減少 | 89(40.8) | 10(4.6) | 67(29.9) | 2(0.9) |
| 骨痛 | 64(29.4) | 13(6) | 85(37.9) | 12(5.4) |
| 背部痛 | 50(22.9) | 4(1.8) | 43(19.2) | 2(0.9) |
| 悪心 | 60(27.5) | 1(0.5) | 17(7.6) | 2(0.9) |
| 食欲減退 | 45(20.6) | ー | 31(13.8) | 2(0.9) |
| 貧血 | 49(22.5) | 13(6) | 24(10.7) | 5(2.2) |
| 下痢 | 48(22) | 1(0.5) | 19(8.5) | 1(0.4) |
| 無力症 | 39(17.9) | 3(1.4) | 25(11.2) | 4(1.8) |
| 関節痛 | 34(15.6) | ー | 25(11.2) | ー |
| 便秘 | 32(14.7) | ー | 27(12.1) | ー |
| 体重増加 | 26(11.9) | ー | 25(11.2) | 1(0.4) |
| ほてり | 21(9.6) | ー | 30(13.4) | ー |
| 好中球減少症 | 24(11) | 10(4.6) | 1(0.4) | ー |
顎⾻壊死(グレード1以上)が17例に報告された︓エンザルタミド+ゾーフィゴ併用群で14例(6.4%)、エンザルタミド単独群で3例(1.3%)であった。
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、 バイエルから講演料・コンサルタント料等を受領した者が含まれる。)
注:骨折に関わる有害事象における「緊急安全通知書発出前後」の項目は事後解析であるが、安全性情報であることを考慮し情報提供する。(緊急安全通知書発出日:2018年3月14日)
- ・ 安全性解析対象集団における骨折の発現状況は以下のとおりであった。
| エンザルタミド+ゾーフィゴ併用群 (n=218) | エンザルタミド単独群 (n=224) | |
|---|---|---|
| 骨折発現症例*1、n(%) | 59(27.1) | 32(14.3) |
| 骨折発現症例の登録時期 | ||
| 緊急安全通知書発出前注、n(%) | 30(50.8) (登録患者56例中の53.6%) | 12(37.5) (登録患者59例中の20.3%) |
| 緊急安全通知書発出後注、n(%) | 29(49.2) (登録患者162例中の17.9%) | 20(62.5) (登録患者165例中の12.1%) |
| 観察期間中の骨修飾薬の使用(骨折のための使用を除く) | ||
| なし、n(%) | 24(40.7) | 13(40.6) |
| あり、n(%) | 35(59.3) | 19(59.4) |
| 初回骨折時期 | ||
| 治療期間*2中、n(%) | 47(79.7) | 23(71.9) |
| 治療期間*2後、n(%) | 12(20.3) | 9(28.1) |
-
*1: 症状の有無または病因を問わず、プロトコルで規定した試験治療中または試験治療後に発生した全骨折を評価対象とした。複数回の発現例は1例としてカウントした。
骨折事象の発現は、エンザルタミド+ゾーフィゴ併用群の59例で85件、エンザルタミド単独群の32例で40件であった。 - *2: 試験治療薬投与開始日から最終投与後28日まで
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026. (本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、バイエルから講演料・コンサルタント料等を受領した者が含まれる。)より改変
| エンザルタミド+ゾーフィゴ併用群 (安全性解析対象集団: n=218) | エンザルタミド単独群 (安全性解析対象集団: n=224) | |||||
|---|---|---|---|---|---|---|
項目 グレード† | 全グレード | グレード≥3 | グレード5 | 全グレード | グレード≥3 | グレード5 |
| 鎖骨骨折 | 1(0.4) | |||||
| 肋軟骨骨折 | 1(0.4) | |||||
| 大腿骨頸部骨折 | 1(0.4) | |||||
| 大腿骨骨折 | 2(0.9) | 2(0.9) | ||||
| 腓骨骨折 | 1(0.5) | |||||
| 足骨折 | 2(0.9) | |||||
| 骨折 | 3(1.4) | 2(0.9) | ||||
| 仙骨骨折 | 2(0.9) | |||||
| 手骨折 | 1(0.5) | |||||
| 股関節部骨折* | 1(0.5) | 1(0.5) | ||||
| 上腕骨骨折 | 1(0.4) | |||||
| 腰椎骨折 | 4(1.8) | 2(0.9) | ||||
| 膝蓋骨骨折 | 1(0.5) | |||||
| 骨盤骨折 | 1(0.5) | |||||
| 橈骨骨折 | 1(0.4) | |||||
| 肋骨骨折 | 13(6) | 5(2.2) | ||||
| 肩骨折 | 1(0.5) | |||||
| 脊椎圧迫骨折 | 4(1.8) | 1(0.5) | 1(0.4) | |||
| 脊椎骨折* | 4(1.8) | 1(0.5) | 2(0.9) | 1(0.4) | ||
| 胸骨骨折 | 1(0.4) | |||||
| 胸椎骨折 | 1(0.5) | |||||
| 歯牙破折 | 1(0.5) | |||||
| 外傷性骨折 | 1(0.4) | |||||
| 尺骨骨折 | 1(0.5) | 1(0.5) | ||||
| 上肢骨折 | 1(0.4) | |||||
| 手首関節骨折* | 2(0.9) | |||||
| 骨粗鬆症性骨折 | 1(0.5) | |||||
| 病的骨折** | 14(6.4) | 4(1.8) | 12(5.4) | 2(0.9) | ||
#:治療期間中(初回投与日~最終投与28日後)に記録された有害事象のうち“Fracture”と付く事象名をTable S6より抜粋[治療期間後も含めて骨折のあった患者数をカウントしたTable 1(1症例中複数の骨折があった場合は1と集計)とは数値が一致しない]、†:CTCAE version 4.03 による評価、*:別途独立したCTCAE Grading基準を有する、**:Pathological Fractureと記録されたもの以外にも病的骨折が含まれる可能性がある
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、 バイエルから講演料・コンサルタント料等を受領した者が含まれる。)より作表
国外第Ⅲ相試験(PEACE-3試験)で、無症候性または軽度症候性の骨転移を有するCRPC患者446例を対象に、エンザルタミド単独療法に対するエンザルタミド+ゾーフィゴ併用療法の有用性が検討された。
PEACE-3試験におけるrPFS、OSの結果は以下のとおりであった。
- rPFS[主要評価項目、検証的解析結果]
エンザルタミド単独群に対するエンザルタミド+ゾーフィゴ併用群の優越性が検証された(ハザード比 0.69、p=0.0009、層別*1log-rank test)。
中央値:エンザルタミド+ゾーフィゴ併用群19.4ヵ月、エンザルタミド単独群16.4ヵ月
- OS[重要な副次評価項目、最終解析結果]
エンザルタミド+ゾーフィゴ併⽤群は、エンザルタミド単独群よりも延⻑した(ハザード比 0.76、p=0.0096*2、層別*1log-rank test )。
中央値:エンザルタミド+ゾーフィゴ併用群38.2ヵ月、エンザルタミド単独群32.6ヵ月
*1:ベースライン時の疼痛スコア、ドセタキセル治療歴、ランダム化時に報告された骨修飾薬の使用状況
*2:最終解析の有意水準:0.0248
PEACE-3試験における安全性の主な結果は以下のとおりであった。
- 有害事象(全グレード)の発現率は、エンザルタミド+ゾーフィゴ併用群218例中218例(100%)、エンザルタミド単独群224例中219例(97.8%)であり、エンザルタミド+ゾーフィゴ併用群の主な有害事象(全グレード)は高血圧122例(56.0%)、体重減少89例(40.8%)、疲労86例(39.4%)、骨痛64例(29.4%)、悪心60例(27.5%)などであった。
- 骨折*の発現は、エンザルタミド+ゾーフィゴ併用群で59例(27.1%)、エンザルタミド単独群で32例(14.3%)であった。
*:試験治療中または試験治療後、症状の有無や病因、または骨修飾薬使用の有無を問わない
エンザルタミドとゾーフィゴの併用療法は、
エンザルタミド処方対象の骨転移のみを有するCRPC患者の一次治療の選択肢の1つとしてご検討をお願いします。
Tombal B, et al.: Ann Oncol. 36; 1058-1067, 2025.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。)
Gillessen S, et al.: Ann Oncol. Articles in Press, Feb 26, 2026.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者には、バイエルから講演料・コンサルタント料等を受領した者が含まれる。)
主な選択基準(抜粋)1,2)
- 組織学的に前立腺腺癌と確定診断された患者
- 無症候性または軽度症候性(BPI WP24:簡易疼痛質問票の項目3(直近24時間の最悪疼痛)のスコア(0~10)が4未満)
- 骨転移が4ヵ所以上*1認められた患者(リンパ節転移の有無は問わない)
- 多病巣性骨病変を有する患者(superscanを有する患者は除外)
- 以下のいずれかのPCWG3に基づく進行性CRPCの定義を満たす患者
- PSA値上昇のみの進行:1週間以上間隔をあけた測定でPSA値の上昇が連続して確認され、最終値が2ng/mL超の患者
- 骨病変の進行:PSA上昇による進行にかかわらず、2つ以上の新たな骨病変の出現が確認された患者
- リンパ節病変の進行:PSA上昇による進行にかかわらず、RECIST 1.1に準拠した進行が確認された患者
- WHO Performance status 0-1
- 過去12ヵ月以内のDEXA検査のTスコア ≧ -2.5[骨粗鬆症3)の除外のため]*2
- 血清テストステロン<50ng/dL
- 両側精巣摘出または試験期間中にLHRHアゴニストまたはアンタゴニストによるADTを継続している患者
- 十分な骨髄機能(好中球絶対数≧1.5×109/L、血小板数≧100×109/L、ヘモグロビン≧10.0g/dL)を有する患者
- 前治療または併用療法
- ドセタキセルの前治療は、去勢感受性の状態で投与され、ADT開始後4ヵ月以内に開始された場合は許容(注:CRPCに対してドセタキセル治療歴のある患者は除外)
- mCSPCに対してアビラテロンを投与され、1年以上奏効または病勢が安定していた場合、アビラテロンの前治療は許容(注:CRPCに対してアビラテロン治療歴のある患者は除外)
- アビラテロンによる前治療は、ランダム化の少なくとも4週間前に中止されていれば許容
- ビカルタミドまたはフルタミドによる前治療は、ランダム化の少なくとも48時間前に中止されていれば許容
*1:2018年に、2ヵ所以上から4ヵ所以上に変更
*2:2018年に追加された
主な除外基準(抜粋)1)
- 内臓転移を有する患者
- CRPCに対してドセタキセル治療歴のある患者
- CRPCに対してアビラテロン治療歴のある患者
- エンザルタミド、アパルタミド、ニュベクオ及びゾーフィゴによる前治療歴のある患者
- CYP17阻害剤(アビラテロン、orteronel*3)との併用療法を受けている患者およびケトコナゾールを併用している患者
- 半身外部放射線治療歴のある患者。他の種類の外部放射線治療を受けた患者は、骨髄機能を評価し、ヘモグロビン、絶対好中球数、血小板のプロトコル要件を満たしている場合は許容
- 他の放射性核種による治療歴のある患者
- 痙攣発作の既往歴のある患者
- エンザルタミドまたはゾーフィゴに関連する化合物に対する既知の過敏症がある患者
*3:国内未承認
-
1) Tombal B, et al.: Ann Oncol. 36; 1058-1067, 2025.(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。
著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。) - 2) Gillessen S, et al.: Eur Urol. 87: 285-288, 2025(本試験は医師主導臨床試験であり、バイエルは試験費用の一部と製剤を提供した。著者にはバイエルより講演料・コンサルタント料等を受領している者が含まれる。)
- 3) WHO Techincal Report Series 843

![初回骨折までの期間[安全性評価項目]](/sites/g/files/vrxlpx13761/files/2026-03/doctor_product_performance_peace3-img-new-04.png)
